Адреногенитальный синдром
Содержание:
- Признаки и симптомы
- Формы адреногенитального синдрома
- Симптомы адреногенитального синдрома
- Симптомы адреногенитального синдрома
- Причины адреногенитального синдрома
- Методы диагностики адреногенитального синдрома
- Диагностика
- Механизм развития
- Классификация
- Лечение адреногенитального синдрома
- Причины адреногенитального синдрома
Признаки и симптомы
Проявления зависят от характера повреждений гена и выраженности ферментной недостаточности, при этом определить пол новорожденного не всегда возможно без генетического тестирования.
Симптомы будут различаться в зависимости от типа врожденной гиперплазии надпочечников и времени появления при диагностике расстройства.
• Дети с неклассической (постпубертатной, благоприятной) формой могут не иметь признаков врожденной гиперплазии надпочечников, а диагноз устанавливают только в подростковом возрасте.
• У девочек с более тяжелыми формами (сольтеряющая и простая вирильная) часто встречаются аномальные половые органы уже при рождении (женский псевдогермафродитизм), что позволяет заподозрить патологию до появления симптомов. Аномалии развития гениталий включают полное или частичное слияние , половых губ, клиторомегалию (увеличение клитора), формирование урогенитального синуса, углубленное преддверие влагалища.
• Новорожденные мужского пола визуально могут не иметь каких-либо отклонений, даже при тяжелой форме расстройства.
У детей с выраженным дефицитом 21-гидроксилазы при сольтеряющей форме симптомы развиваются в течение 2 или 3 недель после рождения, для данного варианта врожденного адреногенитального синдрома и у мальчиков, и у девочек характерны:
• отказ от питания, рвота, диарея; • неспособность к росту и развитию; • дегидратация; • гипотония (низкое кровяное давление); • нарушения электролитного баланса: аномальные уровни натрия (гипонатриемия) и калия (гиперкалиемия) в крови, судороги; • избыточная пигментация кожи; • аномальный сердечный ритм.
Если патология не диагностирована своевременно и не начата гормональная терапия, может развиться надпочечниковый кризис, угрожающий жизни.
Часто состояние мальчиков ошибочно принимают за последствия пилорического стеноза и гастроэнтерита, что приводит к смерти из-за отсутствия приема глюкокортикоидов.
У девочек с постпубертатной (более мягкой формой, по сравнению с сольтеряющей и простой вирильной) сохранены нормальные женские половые органы (влагалище, яичники, матка и фаллопиевы трубы).
По мере взросления появляются:
• нарушения менструального цикла по типу олигоменореи, поздний приход менархе (первой менструации); • недоразвитие молочных желез; • раннее появление оволосения лобковых, подмышечных зон; • чрезмерный рост волос на теле и на лице; угревая сыпь и гиперсекреция сальных желез; • увеличение клитора.
При простом вирильном адреногенитальном синдроме менструации, несмотря на все признаки раннего (до 7 лет) полового созревания отсутствуют, недоразвитие молочных желез, диспропорции тела, низкий рост. Выраженная вирилизация: увеличение клитора, формирование кадыка, грубый голос и пр.
У мальчиков с наступлением полового созревания симптомы включают:
• низкий тембр голоса; • большой половой член при яичках нормального размера; • выраженные вторичные половые признаки; • усиление гиперпигментации мошонки; • хорошее развитие мускулатуры.
При биопсии яичка у мужчин обнаруживают незрелые канальцы и отсутствие клеток Лейдига, что может проявляться бесплодием.
В детском возрасте девочки и мальчики выше сверстников, но рост взрослых с адреногенитальным синдромом значительно ниже, чем у здоровых людей. Исключение — постпубертатная форма, при которой признаки надпочечниковой недостаточности проявляются позднее. Изменения пропорций тела включают узкий таз, широкие плечи, укороченные конечности, развитую мускулатуру.
Формы адреногенитального синдрома
Во всемирной практике эндокринологи используют клиническую классификацию адреногенитального синдрома, согласно которой выделяется одна основная, или классическая форма заболевания и две неклассические формы с легким течением клинической картины. Формирование фенотипических признаков этой редкой патологии имеет четкую связь со степенью недостаточности фермента 21-гидроксилазы и сопутствующей гиперандрогенией.
Врожденный адреногенитальный синдром, протекающий в классической форме, провоцируется изменениями функционирования надпочечников еще в период их закладки в период внутриутробного развития плода. В связи с тем, что избыточная продукция андрогенов оказывает непосредственное влияние на формирование первичных половых признаков, происходит полное развитие внутренних органов малого таза по женскому типу, в то время как процесс формирования наружных половых органов находится на начальной стадии развития.
В дальнейшем избыточное влияние тестостерона провоцирует вирилизацию только наружных половых органов у плода женского пола, то есть происходит увеличение полового бугорка, который превращается в клитор пенисообразной формы, сливание лабиосакральных складок и формирование псевдомошонки, нарушение разделения урогенитального синуса на влагалище и уретру. Такой тип вирилизации затрудняет определение правильного пола ребенка после рождения.
Помимо изменений формы и функционирования половых органов, у ребенка наблюдается гиперплазия надпочечников, обусловленная избыточной продукцией андрогенов с начала закладки надпочечников.
Адреногенитальный синдром у детей, протекающий в классической форме, является обоснованием для динамического наблюдения у педиатра-эндокринолога, который определяет оптимальный возраст пациента для проведения хирургической пластики аномалии развития и дальнейшего медикаментозного лечения, направленного на развитие ребенка по женскому типу.
В ситуации, когда врожденный дефект фермента 21-гидроксилазы, не оказал влияние на функционирование надпочечников в период развития плода, существует еще один критический период развития фенотипических признаков адреногенитального синдрома – период пубертатного развития. В связи с этим, данная форма адреногенитального синдрома имеет второе название «пубертатная».
Дебют развития клинических симптомов приходится на период адренархе, который наступает за 3 года до наступления менструаций и заключается в раннем развитии вторичных половых признаков, избыточном оволосении и пубертатном «скачке роста». Для данной категории пациентов характерным признаком является отставание периода наступления первых менструаций, который приходится на возраст 16 лет. У девочек с адреногенитальным синдромом период нормализации менструального цикла занимает очень продолжительный отрезок времени.
Пациентки с пубертатной формой адреногенитального синдрома имеют характерные фенотипические признаки, отличающие их от сверстниц (жирный тип кожи со склонностью к появлению акнэ фолликулярного типа, избыточное стержневое оволосение кожных покровов, высокий рост и широкие плечи, гипоплазия молочных желез). Опытный эндокринолог уже после первичного осмотра пациентки может установить верный диагноз.
При возникновении избыточной продукции андрогенов после периода полового созревания, а именно в возрасте после двадцати лет, девушек беспокоит невозможность зачатия ребенка и частые эпизоды самопроизвольных выкидышей на раннем сроке беременности. Трудности зачатия объясняются нерегулярностью менструального цикла со склонностью к удлинению межменструального периода. Грубого изменения фенотипа при данной патологии не наблюдается и установление диагноза возможно только после всестороннего обследования пациентки с применением лабораторных и инструментальных методик.
Симптомы адреногенитального синдрома
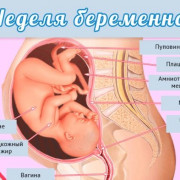
При врожденной форме адреногенитального синдрома еще в период внутриутробного развития при формировании гормональной функции надпочечников вырабатывается излишнее количество андрогенов. Избыток андрогенов приводит к возникновению половой дифференцировки, относящейся к плоду женского пола. К 9-11 неделе внутриутробного развития плод уже имеет половое строение и органы, характерные для женского организма, хотя наружные половые органы на данном этапе еще только начинают формироваться. При этом женский фенотип формируется из начального типа.
На женский плод и его наружные половые органы оказывает влияние чрезмерная выработка тестостерона, в итоге происходит значительное увеличение полового бугорка, который затем принимает форму пенисообразного клитора, лабиосакральные складки сливаются и по форме напоминают мошонку. Урогенитальный синус открывается под деформированным клитором, не распределяясь изначально на влагалище и уретру. Поэтому при рождении ребенка зачастую неправильно определяют его половую принадлежность. Так как гонады яичники приобретают женскую форму, врожденный адреногенитальный синдром нередко называют ложным женским гермафродитизмом, в период внутриутробного развития гиперпродукция андрогенов приводит к гиперплазии надпочечников.
Дети, страдающие таким заболеванием, нуждаются в постоянном контроле со стороны детских эндокринологов. Современные медицинские методики предусматривают своевременное хирургическое лечение адреногенитального синдрома, чтобы операционным путем произвести коррекцию пола и в дальнейшем ребенок развивался по женскому типу. Сейчас к гинекологам-эндокринологам нередко обращаются пациентки, у которых адреногенитальный синдром характеризуется поздней формой.
При пубертатной врожденной форме дефицит С21-гидроксилазы проявляется в период внутриутробного развития еще во время пубертатного периода, когда только проявляется гормональная функция коры надпочечников. Однако нарушения особенно заметны непосредственно перед наступлением у девочки первой менструации. И если обычно в популяции первая менструация протекает в 12-13 лет, то у девочек с врожденным адреногенитальным синдромом, характеризующимся пубертатной формой, первая менструация наступает значительно позже, лишь в 15-16 лет.
Менструальный цикл при данном заболевании достаточно неустойчив, менструации протекают нерегулярно, у девочек возникает тенденция к олигоменорее. Промежуток между менструациями значительный, как правило, он составляет 30-45 дней.
Гирсутизм довольно ярко выражен, довольно часто он проявляется в росте стержневых волос, расположенных по белой линии живота, в росте волос над верхней губой по мужскому принципу, на бедрах и вокруг сосков. На теле появляется большое количество сальных желез, нередко наблюдается нагноение волосяных фолликулов, кожа на лице становится жирной, поры увеличиваются и расширяются. Девушки, страдающие пубертатной формой адреногенитального синдрома, отличаются довольно высоким ростом и мужским телосложением, широкими плечами и узким тазом, наблюдается гипопластичность молочных желез. Как правило, главными жалобами таких пациенток при обращении к медикам становится возникновение угревой сыпи либо жалобы на нерегулярный менструальный цикл.
При данной постпубертатной форме заболевания симптомы адреногенитального синдрома у девушек заметны лишь после полового созревания. Довольно часто симптомы становятся ярко выраженными после медицинского аборта, во время неразвивающейся беременности либо после самопроизвольного выкидыша. Выражается в нарушении менструального цикла, промежутки между менструациями значительно увеличиваются, менструальные выделения становятся скудными, нередко возникают задержки.
В данном случае гиперандрогения характеризуется относительно мягкими признаками проявления, гирсутизм почти не выражен и проявляется лишь в незначительном оволосении на белой линии на животе, немного волос может быть на голенях, около сосков, либо над верхней губой. Молочные железы у девушки развиваются таким же образом, как у ее сверстниц, телосложение формируется по женскому типу, метаболических нарушений не проявляется.
Симптомы адреногенитального синдрома
Симптомов адреногенитального синдрома достаточно много, зависеть они могут от преимущественной формы.
Среди них следует выделить основные проявления, типичные для всех форм:
- дети раннего возраста характеризуются высоким ростом и большой массой тела. Постепенно идёт изменение внешнего вида. К подростковому периоду наблюдается остановка в росте, масса тела подвергается нормализации. Во взрослом возрасте, люди, страдающие адреногенитальным синдромом, имеют низкий рост и худощавое телосложение;
- гиперандрогения характеризуется большими размерами полового члена и небольшими яичками у лиц мужского пола. У девочек адреногенитальный синдром проявляется пенисообразным клитором, оволосением имеющим преимущественно мужской тип (см. фото выше). Кроме того, девочки имеют признаки гиперсексуальности и грубого голоса;
- на фоне быстрого роста наблюдается выраженная деформация опорно—двигательной системы;
- люди характеризуются нестабильностью в психическом состоянии;
- в области кожных покровов имеются участки гиперпигментации;
- периодически появляется судорожный синдром.
При простой форме адреногенитальный синдром у мальчиков проявляется:
- увеличенным в несколько раз половым членом;
- мошонка приобретает выраженную гиперпигментацию, так же как и анальная область;
- отмечается выраженный гипертрихоз;
- уже в детском возрасте возникает эрекция;
- голос у мальчика грубый, имеет низкий тембр;
- на кожных покровах появляются вульгарные угри;
- идёт выраженная преждевременная маскулинизация и ускоренное формирование костной ткани.;
- рост может быть достаточно низким.
Постпубертатный врожденный адреногенитальный синдром проявляется:
- поздним наступлением менструации;
- менструальный цикл характеризуется выраженной нестабильностью, с нарушенной периодичностью и длительностью.имеется склонность к олигоменорее;
- отмечается избыточное оволосение, преимущественно по мужскому типу;
- кожа становится более жирной, расширяются поры в области лица;
- телосложение мужеподобное, характеризуется развитием широких плеч и узким тазом;
- молочные железы имеют небольшой размер, чаще это лишь кожная складка с недоразвитым соском.
Вирильная форма:
Характеризуется тем, что строение наружных половых органов имеет интерсексуальные признаки.
- клитор имеет большие размеры, в области головки имеется экстензия уретры;
- размер и форма половых губ напоминает мошонку;
- в области мошонки и подмышечных впадин определяется избыточное оволосение;
- адреногенитальный синдром у новорожденных не всегда позволяет идентифицировать половую принадлежность. Девочки имеют большую внешнюю схожесть с мальчиками. В области молочных желёз в пубертатном периоде не отмечается роста.
Сольтеряющая форма:
- характеризуется у ребёнка наблюдается медленный прирост массы.
- сразу после рождения появляется сильная рвота, носящая повторный характер, аппетит отсутствует, в области живота появляются сильные боли с напряжением передней брюшной стенки, после каждого кормления срыгивание;
- достаточно быстро развивается обезвоживание, при котором снижается натрий, а калий повышается;
- ребёнок в течение нескольких суток становится вялым, перестаёт нормально сосать, сознание переходит в коллаптоидное вплоть до того, что развивается кардиогенный шок и возможный летальный исход при несвоевременно оказанной помощи.
Причины адреногенитального синдрома
Это заболевание относится к наследственным. У больного нарушается образование кортизола и альдостерона надпочечниками. Это происходит из-за дефекта ферментов, участвующих в синтезе стероидных гормонов.
Некоторые типы болезни имеют выраженные признаки с рождения, а в других случаях имеются скрытые, «молчащие» гены, которые проявляются при стрессовых ситуациях в подростковом периоде или детородном. Провокаторами могут быть травмы, радиация, стресс, отравления, тяжелые инфекции, физические перенапряжение. Ранее эти формы патологии считали приобретенными, а затем нашли дефектные гены, полученные от родителей. Причины мутаций остались пока неисследованными.
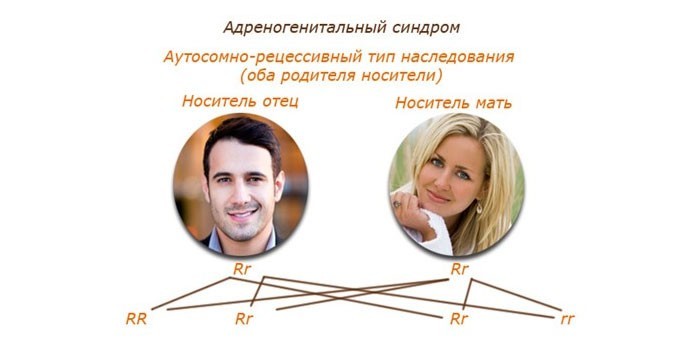
Так как ген, отвечающий за адреногенитальный синдром, является рецессивным (подавленным), то для того, чтобы заболевания проявилось, необходимо его наличие у обоих родителей. Причем один из них может быть болен, а у другого обнаруживается носительство гена.
А здесь подробнее о болезни и синдроме Иценко-Кушинга.
Методы диагностики адреногенитального синдрома
Диагностика в период внутриутробного развития
При обследовании беременных о возможности гиперплазии надпочечников может свидетельствовать аномальное формирование половых органов плода. Это можно увидеть на втором скрининговом акушерском УЗИ. В таких случаях рекомендуется дополнительное обследование, назначается анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ).
Диагностика после родов
После родов диагностика не представляет сложности. Назначается обследование: проба с АКТГ – нет повышения содержания кортизола после его введения; анализ крови – снижен натрий, повышен калий, 17 ОН-прогестерон в 5-7 раз и более, андростендион (предшественник стероидов), ренин (при сольтеряющей форме); анализ мочи – высокая концентрация 17-кетостероидов, после приема преднизолона снижается наполовину. В сомнительных случаях применяют кариотипирование для подтверждения женского кариотипа (46ХХ). Исследование мутаций в гене CYP11B1 – секвенирование на выявление мутации – His R448H.
Диагностика при позднем клиническом дебюте
Большее значение диагностический поиск приобретает при позднем клиническом дебюте или скрытом течении с минимальными внешними проявлениями вирилизации. В подобных ситуациях для выявления адреногенитального синдрома используют следующие лабораторные и инструментальные методы:
-
гормональный профиль (кортизол и предшественники, 17-ОНП, ДЭА-с и ДЭА, АКТГ и др.);
-
рентгенография костей кисти (раннее завершение роста);
-
УЗИ органов малого таза (признаки ановуляторного цикла), надпочечников (гиперплазии); в ряде случаев назначается МРТ, МСКТ исследование;
-
измерение базальной температуры. Температурная кривая типична для ановуляторного цикла: первая фаза растянута, вторая укорочена, что обусловлено недостаточностью желтого тела, которое не образуется из-за отсутствия овуляции).
Дифференциальная диагностика адреногенитальных расстройств, возникших в пубертатном и детородном возрасте, проводится с синдромом поликистозных яичников, овариальными андробластомами, андростеромами надпочечников, вирильным синдромом гипоталамического происхождения и конституциональным гирсутизмом. В сложных случаях к диагностике привлекают эндокринологов, урологов, врачей-генетиков.
Чтобы точно продиагностировать заболевание, запишитесь на прием к специалистам сети «Семейный доктор».
Диагностика
Постановка диагноза при антенатальных типах АГС с характерными изменениями половых органов не представляет сложности и проводится сразу после родов. В сомнительных случаях применяют кариотипирование для подтверждения женского кариотипа (46ХХ). Большее значение диагностический поиск приобретает при позднем клиническом дебюте или скрытом течении с минимальными внешними проявлениями вирилизации. В подобных ситуациях для выявления адреногенитального синдрома используют следующие лабораторные и инструментальные методы:
- Уровень 17-ОН-прогестерона. Высокая концентрация 17-гидроксипрогестерона, который является предшественником кортизола — ключевой признак недостаточности 21-гидроксилазы. Его содержание увеличено в 3-9 раз (от 15 нмоль/л и выше).
- Стероидный профиль (17-КС). Повышение уровня 17-кетостероидов в моче у женщин в 6-8 раз свидетельствует о высоком содержании андрогенов, производимых корой надпочечников. При выполнении преднизолоновой пробы концентрация 17-КС уменьшается на 50-75%.
- Содержание андростендиона в сыворотке крови. Повышенные показатели этого высокоспецифичного метода лабораторной диагностики подтверждают усиленную секрецию предшественников мужских половых гормонов.
- Уровень АКТГ в крови. Для классических форм заболевания характерна компенсаторная гиперсекреция адренокортикотропного гормона передней долей гипофиза. Поэтому при синдроме вирилизирующей дисфункции показатель повышен.
- УЗИ яичников. В корковом веществе определяются фолликулы на разных стадиях созревания, не достигающие преовуляторных размеров. Яичники могут быть несколько увеличены, однако разрастания стромы не наблюдается.
- Измерение базальной температуры. Температурная кривая типична для ановуляторного цикла: первая фаза растянута, вторая укорочена, что обусловлено недостаточностью желтого тела, которое не образуется из-за отсутствия овуляции.
Для сольтеряющего варианта АГС также характерна повышенная концентрация ренина в плазме крови. Дифференциальная диагностика адреногенитальных расстройств, возникших в пубертатном и детородном возрасте, проводится с синдромом поликистозных яичников, овариальными андробластомами, андростеромами надпочечников, вирильным синдромом гипоталамического происхождения и конституциональным гирсутизмом. В сложных случаях к диагностике привлекают эндокринологов, урологов, врачей-генетиков.
Механизм развития
Генетический дефект передается по аутосомно-рецессивному типу. Синдром главным образом возникает вследствие недостаточной выработки 21-гидроксилазы.
В остальных случаях дефект ДНК приводит к нарушению производства других ферментов, участвующих в стероидогенезе – 3-β-гидроксистероиддегидрогеназы, 22-десмолазы, синтетазы альдостерона и др
Важно понимать, причины отклонений носят сугубо наследственный характер. Факторами риска синдрома принято считать:
- повышенный уровень ионизирующего излучения;
- прием сильнодействующих препаратов;
- острое либо хроническое радиационное отравление;
- интеркуррентные патологии;
- длительное использование гормональных контрацептивов;
- хирургическое вмешательство;
- дисфункция щитовидной железы;
- аборты;
- патологии почек;
- опухолевый процесс;
- травмы;
- стрессы.
В основе механизма развития классического (врожденного) варианта адреногенитальных нарушений лежит принцип обратной связи, начальным звеном которой является недостаток стероидов. Несостоятельность процесса гидроксилирования сопровождается неполным превращением прогестерона, а также 17-гидроксипрогестерона в дезоксикортикостерон и 11-дезоксикортизол. В результате уровень кортизола снижается. При этом усиливается выработка адренокортикотропного гормона (АКТГ), который, собственно, и вызывает компенсаторную гиперплазию коры надпочечников.
Риск наследования патологии
Вероятность рождения ребенка с адреногенитальным расстройством при носительстве патологического гена у обоих родителей составляет 25%, а в браке носителя и больного – 75%. При ситуации, когда один партнер имеет полноценное ДНК, клинические проявления синдрома у детей не обнаруживаются. Крайне редко адреногенитальные нарушения наследуются спорадически. Внезапное появление признаков синдрома, как правило, обусловлено нарушениями в процессе формирования женских и мужских репродуктивных клеток.
Классификация
Для удобства постановки диагноза, в медицинской практике адреногенитальный синдром условно классифицируется на несколько основных форм, среди которых выделяют:
- Сольтеряющая форма. Данная разновидность заболевания является наиболее распространенной. Чаще всего, сольтеряющий адреногенитальный синдром диагностируется в периоде новорожденности, а также у детей в возрасте до 1 года. Для данного состояния характерно нарушение гормонального баланса и функциональная недостаточность коры надпочечников. В момент обследования таких детей, выявляется снижение альдостерона до минимальных показателей. Гормон альдостерон обеспечивает баланс воды и электролитов в организме человека, поэтому его нехватка приводит к функциональным расстройствам сердечно-сосудистой системы, а также к нестабильности показателей артериального давления.
- Вирильная форма. Данное состояние относится к классическим вариантам течения адреногенитального синдрома. В данной ситуации не наблюдается недостаточность надпочечников. Изменения затрагивают только область наружных половых органов. Клинические проявления вирильный формы адреногенитального синдрома дают о себе знать с самого момента рождения. Какие-либо другие изменения в органах и системах при этом отсутствуют.
- Постпубертатная форма. Данная форма адреногенитального синдрома относится к неклассической форме ВДКН, и, как правило, диагностируется чаще у женщин с повышенной сексуальной активностью. К наиболее вероятным причинам возникновения данного состояния, относят не только генные мутации, но и опухоли корковой части надпочечников. Постпубертатная форма адреногенитального синдрома является одной из потенциальных причин развития бесплодия.
Лечение адреногенитального синдрома
Лабораторное и инструментальное подтверждение диагноза является обоснованием для проведения адекватной заместительной гормональной терапии с применением препаратов глюкокортикостероидного ряда.
Назначение любого глюкокортикостериода обязательно должно быть строго дозировано и подконтрольно лабораторным показателям крови и мочи. Применение Дексаметазона в суточной дозе 0,25 мг следует производить до момента устранения основных клинических проявлений заболевания (нормализация цикличности базальной температуры, устранение дисменореи, эхоскопически подтвержденное устранение мультифолликулярности яичников). Абсолютным критерием положительной эффективности гормонотерапии в этом случае является наступление запланированной беременности, однако данный факт не является показанием для прерывания приема препарата. Дексаметазон в период беременности целесообразно применять до момента формирования плаценты, которая обеспечивает нормализацию гормонального статуса плода.
Женщины, у которых период наступления беременности совпал с приемом гормональных препаратов глюкокортикоидного ряда, подлежат госпитализации в стационар с целью проведения динамического ультразвукового исследования, а также определения концентрации 17-кетостероидов в моче. Наличие у беременной женщины, принимающей гормональную терапию с целью лечения адреногенитального синдрома, самопроизвольных абортов в анамнезе является обоснованием для назначения эстроенсодержащих гормональных средств, действие которых направлено на улучшение поступления оксигенированной крови к развивающемуся плоду. Среди широкого спектра этой группы лекарственных средств наибольшее распространение получил Микрофоллин, эффективность которого максимальная в терапевтической дозе 0,25 мг в сутки. Появление у женщины кровянистых выделений или тянущих болей в нижней части живота является показанием к отмене препарата.
В связи с тем, что женщины, страдающие адреногенитальным синдромом, имеют проблемы с вынашиванием плода и склонность к возникновению самопроизвольного выкидыша на раннем сроке беременности, целесообразным в данной ситуации является назначение природного аналога прогестерона «Дюфастона» в суточной дозе 20 мг. Длительный прием данного препарата устраняет истмикоцервикальную недостаточность, которая является самой распространенной причиной самопроизвольного аборта.
Препаратом, оказывающим стимулирующее влияние на процесс развития овуляции, является Кломифен, применение которого рекомендуется сочетать с глюкокортикоидной терапией. Пациенткам обязательно необходимо соблюдать режим приема препарата, заключающийся в приеме его в суточной дозе 100 мг с третьего по седьмой день менструального цикла каждый месяц до наступления беременности.
В ситуации, когда признаки адреногенитального синдрома дебютировали в зрелом возрасте, когда женщина не заинтересована в сохранении репродуктивной функции, рекомендуется терапия заболевания с применением комбинированных препаратов, содержащих антиандрогены и эстрогены (Андрокур в дозировке 25 мг). Следует учитывать, что данную группу препаратов относят к категории симптоматических, устраняющих незначительные фенотипические проявления заболевания, и при отмене приема препарата возможно обратное развитие болезни.
Для борьбы с гипергисутизмом гормональная терапия не применяется и в данной ситуации эндокринологи прибегают к назначению Верошпирона в суточной дозе 100 мг утром, длительный прием которого значительно уменьшает проявления избыточного оволосения.
Областью применения гормональных препаратов контрацепции, содержащих низкодозированный гестагенный компонент, лишенный андрогенного влияния, является группа пациенток с признаками поздней постпубертатной формы адреногенитального синдрома. Прежде чем применять данную группу препаратов, следует удостовериться в нежелании пациентки сохранять репродуктивную функцию, так как данные гормональные средства при длительном приеме провоцируют развитие аменореи гипогонадотропного типа.
Причины адреногенитального синдрома
В 90-95% случаев патология возникает при повреждении активного гена CYP21-B, который отвечает за синтез 21-гидроксилазы – фермента, влияющего на образование кортизола. В остальных клинических случаях АГС развивается вследствие дефектов ДНК, нарушающих производство других ферментов, обеспечивающих стероидогенез, – StAR/20,22-десмолазы, 3-β- гидрокси-стероиддегидрогеназы, 17-α-гидроксилазы/17,20-лиазы, 11-β-гидроксилазы, P450-оксидоредуктазы и синтетазы альдостерона.
Различают следующие виды адреногенитального синдрома:
-
сольтеряющий тип. Проявления болезни начинают обнаруживаться с первых недель жизни. У девочек половые органы формируются по мужскому типу, а у мальчиков увеличиваются пенис и мошонка. Из-за грубого нарушения образования стероидных гормонов развивается тяжелая рвота, понос, судороги, темнеет кожа. Прогрессирующее обезвоживание ведет к смерти при отсутствии своевременной заместительной терапии.
Через 2-3 дня от начала клинического проявления заболевания появляются симптомы дегидратации и развития метаболического ацидоза.
-
Простой вирильный. Преобладают нарушения развития половых органов. У девочек: увеличен клитор, похожий на половой член; углублен вход во влагалище; половые губы больше нормы; матка и придатки сформированы. У мальчиков: увеличен пенис, кожа мошонки имеет темную пигментацию. Девочки широкоплечие, с узким тазом, укороченными и массивными конечностями. У них низкий голос, кадык на шее, молочные железы не растут. У мальчиков рано появляются грубые волосы на подбородке и верхней губе, ломается голос.
С возрастом у пациентов нарастают признаки вирилизации вследствие стимулирующего действия андрогенов. Характерно ранее начало полового созревания в 3-5 лет.
-
Постпубертатный тип. Выявляют в молодом возрасте. Приобретенная форма возникает после появления опухоли в надпочечниках или при их повышенной активности.
Половые органы соответствуют полу, но развивается гипертрофия клитора и пениса. Основные нарушения встречаются у женщин – уменьшаются или прекращаются месячные (после стресса, травмы, аборта, выкидыша). Наступление первой менструации может быть только к 15 годам, цикл удлинен (более 30-40 дней). Кожа склонна к повышенной жирности и образованию угрей, имеется повышенное оволосение. При обследовании обнаруживают гиперплазию коркового слоя надпочечников.
Также имеются и варианты неклассического течения адреногенитального синдрома – с высоким давлением крови, с лихорадкой, липидный (ожирение, нарушение холестеринового обмена), с гирсутизмом (усиленный рост волос на теле и лице, по средней линии живота, около сосков).